低浓度含砷As废水可用铁盐沉淀法处理。通常情况下,废水中同时存在三价砷和五价砷,其去除原理为:Fe3++AsO=FeAsO3↓,Fe3++AsO=FeAsO4↓
在紧急情况下,雨水或河水经过煮沸、沉淀处理可饮用。 #生活常识# #应急生存技巧# #食物和水保藏#
题型:填空题 难度:0.4 引用次数:385 题号:13316785
低浓度含砷As废水可用铁盐沉淀法处理。通常情况下,废水中同时存在三价砷和五价砷,其去除原理为:Fe3++AsO=FeAsO3↓,Fe3++AsO=FeAsO4↓。
已知:①三价砷的毒性高于五价砷;
②Ksp(FeAsO3)>Ksp(FeAsO4);
③K2FeO4具有较强的氧化性。pH越小,其氧化性越强,稳定性越弱。
(1)pH约为7时,为除去废水中的砷,下列试剂中去除效果较好的是
(填序号)。
A.FeCl3 B.K2FeO4 C.FeCl3、K2FeO4
选择该试剂的理由是
。
(2)一定条件下,以K2FeO4去除废水中的砷,溶液的pH对砷去除率的影响如图1所示:
①当pH>8时,pH越大,砷去除率越低,其原因可能是
。
②当pH<5时,pH越小,砷去除率越低,其原因可能是
。
(3)Na2S2O8易溶于水、有氧化性,利用Fe—Na2S2O8体系去除废水中的五价砷,反应机理如图2所示。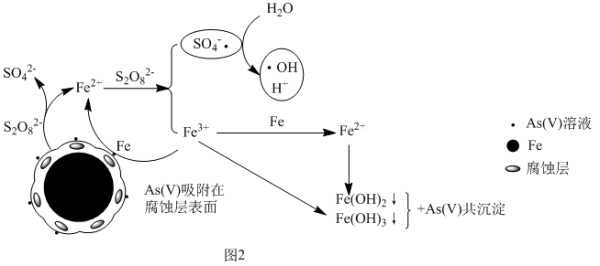
已知:•OH(羟基自由基)是一种不带电荷的活性中间体,“•”表示未成对电子。
①写出•OH的电子式
。
②S2O在此过程中的作用与发生的变化可描述为
。
更新时间:2021/07/10 17:05:15 |
抱歉! 您未登录, 不能查看答案和解析点击登录
相似题推荐【推荐1】I.现有物质:①氢氧化钠固体 ②铜丝 ③氯化氢 ④稀硫酸 ⑤二氧化碳 ⑥氨水 ⑦碳酸钠粉末 ⑧蔗糖晶体 ⑨熔融 ⑩胆矾晶体 ⑪氢氧化铁胶体。溶液请用序号填空:
(1)上述状态下可导电的是
(填序号,下同);属于电解质的是
___________。
(2)⑪的实验室制备方法:向沸水中滴加几滴饱和溶液,加热至液体呈红褐色,停止加热;其化学方程式为
。
Ⅱ.某溶液中只可能含有。当加入一种淡黄色固体并加热时,有刺激性气体放出和白色沉淀产生,加入淡黄色固体的物质的量(横坐标)与析出的沉淀和产生气体的物质的量(纵坐标)的关系如下图所示。

(3)该淡黄色物质做焰色反应实验显黄色。可知溶液中含有的离子是
___________;所含离子的物质的量浓度之比为
___________;所加的淡黄色固体是
___________。
Ⅲ.汽车尾气系统中均安装了催化转化器,可将为其中的和在催化剂的作用下发生反应,生成和。
(4)请写出上述反应的化学方程式并用“双线桥法”表示反应中电子转移的方向和数目:
。当反应转移电子的物质的量为时,氧化剂比还原剂重
___________g。
【推荐3】二氧化碳又名碳酸气,具有较高的民用和工业价值,在多种领域有着广泛的应用。目前,二氧化碳在棚菜气肥、蔬菜(肉类)保鲜、生产可降解塑料等也展现良好的发展前景。二氧化碳是一种无色无味的气体,无毒、不导电并且没有可燃性。但是金属镁在点燃的条件下可以在二氧化碳气体中燃烧。其中还原产物是碳
Ⅰ.①氧化产物是
②请写出化学反应方程式,并用单线桥法表示该反应的电子转移总数
__________Ⅱ.CO2气体与碱溶液反应时,用量不同其生成的产物不同。
①少量CO2通入过量的KOH溶液中,请写出离子反应方程式
②取两份等物质的量浓度等体积的Ca(OH)2的溶液,一份通入过量CO2,生成沉淀的物质的量(n)和通入CO2体积(V)的关系如图所示
写出沉淀变化由a到b的离子方程式:
Ⅲ.另一份先加入少量的KOH固体溶解,再将过量CO2通入KOH和Ca(OH)2的混合溶液中,请绘图表示出生成沉淀的物质的量(n)和通入CO2体积(V)的关系
___________;并写出与图②中不同曲线处对应的离子反应方程式
_____________________________
网址:低浓度含砷As废水可用铁盐沉淀法处理。通常情况下,废水中同时存在三价砷和五价砷,其去除原理为:Fe3++AsO=FeAsO3↓,Fe3++AsO=FeAsO4↓ https://www.yuejiaxmz.com/news/view/214248
相关内容
含砷工业废弃物资源化再利用技术探讨工业上回收利用某合金废料(主要含Fe.Cu.Co.Li等.已知Co.Fe都是中等活泼金属)的工艺流程如下:(1)金属M为Cu.(2)加入H2O2的作用是2Fe2++H2O2+2H+=2Fe3++2H2O.加入氨水的作用是调节溶液的pH使Fe3+转化为Fe(OH)3沉淀.(3)CoC2O4•2H2O高温焙烧的化学方程式为4CoC2O4?2H2O+3O2$\fra 题目和参考答案——青夏教育精英家教网——
工业上以黄铜矿(主要成分CuFeS2)为原料制备金属铜.有如下两种工艺.I.火法熔炼工艺.将处理过的黄铜矿加人石英.再通人空气进行焙烧.即可制得粗铜.(1)焙烧的总反应式可表示为2CuFeS2+ 2SiO2+5O2=2Cu+2FeSiO3+4SO2该反应的氧化剂是 .(2)下列处理SO2的方法.不合理的是 A高空排放 B用纯碱溶液吸收制备亚硫酸钠C用 题目和参考答案——青夏教育精英家教网——
运用还原沉淀法可除去工业废水中含有的Cr2O72
解析生活中常见的饮食误区
工业废水和生活污水可以协同处理吗?
生活废水清洁处理剂的制备方法
[题目]某新型锂离子可充电电池正极材料是含锂的二氧化钴(LiCoO2).充电时LiCoO2被氧化.Li+迁移并以原子形式嵌入电池负极材料碳(C6)中形成LiC6.下列说法正确的是A. 充电时.锂离子电池的负极发生氧化反应B. 放电时.锂离子电池的正极反应为CoO2+Li++e=LiCoO2C. 放电时.锂离子电池的正极的质量逐渐减小D. 充电时.C6极应与 题目和参考答案——青夏教育精英家教网——
铜及其化合物在工业生产和日常生活中有着广泛的应用。(1)Li
威海市住房和城乡建设局 通知公告 威海市生活垃圾焚烧厂扩建工程项目环境影响评价公众参与第二次公示

