某化工厂用3.7t的熟石灰处理溶质质量分数为2%的硫酸废液,待测得废液pH=7时再进行排放。理论上这些熟石灰可以处理硫酸废液质量是多少?
对于石灰墙面裂缝,可用醋酸溶液浸湿,再用石膏填补。 #生活知识# #家庭维修常识# #墙面裂缝处理#
基础巩固 能力提升 变式训练 拓展培优 真题演练 换一批
1.
锂及其化合物在新能源、航天航空等领域应用广泛。从盐湖中提取锂盐的化学方程式为2LiCl + Na2CO3=Li2CO3↓+ 2NaCl。若制得74 kg Li2CO3 , 计算参加反应的LiCl的质量(写出计算过程及结果)。
2.
工业生产中酸性废液直接排放会对环境造成不良影响,如要以中和法处理含氯化氢()7.3吨的酸性废水为中性,请你计算此过程中理论上消耗碱的质量.(提示:碱可自选,需写出计算过程)
3.
某治疗胃酸过多的药片主要成分为碳酸氢钠。为测定药片中碳酸氢钠的含量,将药片研碎,取4.0 g 样品加热到质量不再减少时,收集到的气体经干燥后质量为0.88 g。(碳酸氢钠受热分解的化学方程式为:2NaHCO3 Na2CO3 + H2O + CO2↑,样品中其它成分受热不分解)计算该样品中碳酸氢钠的质量分数。
1.
某化学小组欲用4.9%的稀H2SO4测一瓶标签破损的NaOH溶液的质量分数,取10gNaOH溶液样品,并滴加4.9%的稀硫酸溶液,稀硫酸的滴加量与pH的关系如图所示,求NaOH溶液样品中溶质的质量分数.
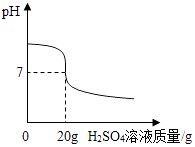
2.
为测定一瓶久置的烧碱样品中氢氧化钠和碳酸钠的质量,取一定质量的该样品充分地溶解于水中,加入足量的氢氧化钙溶液至完全反应,生成10g碳酸钙沉淀。
(2)
已知样品中钠元素的质量为27.6g,计算样品中氢氧化钠的质量
3.
某工厂化验室用10%的氢氧化钾溶液洗涤一定量石油产品中的残余硫酸(该产品中其它物质不与KOH反应),消耗氢氧化钾溶液的质量与反应过程中溶液的pH关系如图所示。
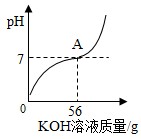
(2)
求石油产品中残余硫酸的质量(写出计算过程)。
1.
有反应: 8A + 3B2 = C2 + 6D(其中A、D是化合物,B2、C2是单质)。若13.6g A与21.3g B2恰好完全反应,生成32.1g D,已知C2的相对分子质量为28,则B的相对原子质量为( )
A . 14 B . 16 C . 32 D . 35.5
2.
现有一包由铁粉、木炭粉、镁粉组成的固体混合物5g,向其中加入一定溶质质量分数的稀盐酸100g,充分反应后过滤,得到滤液103.8g、滤渣1g,下列说法中正确的是( )
A . 生成氢气的质量是0.2g B . 滤液中一定含有氯化镁、氯化亚铁和盐酸 C . 稀盐酸的溶质质量分数小于或等于7.3% D . 若滤渣的成分是木炭粉,则混合物中铁、镁的质量比为7:3
A . 等质量的二氧化硫和三氧化硫中硫元素的质量比为5:4 B . 2.3g某物质在空气中完全燃烧,生成4. 4g二氧化碳和2.7g水,可知该物质只含碳、氢两种元素 C . 用含杂质(杂质不与酸反应,也不溶于水)的铁10 克与50克稀硫酸恰好完全反应后,滤去杂质。所得溶液质量为55.4克,则含杂质铁中铁的质量分数为56% D . 质量和质量分数均相等的氢氧化钠溶液和稀硫酸,充分反应,所得溶液呈酸性
1.
已知某化工厂制得的Na2CO3(俗称:纯碱)粗产品中含有杂质氯化钠,为了测定粗产品中纯碱的纯度,进行了如图装置的实验:
其中E装置中的饱和NaHCO3溶液是为了除去二氧化碳气体中的氯化氢;发生的反应为NaHCO3+HCl═NaCl+H2O+CO2↑.
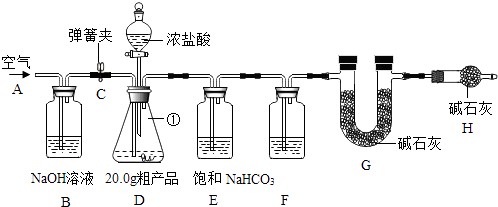
①连接好装置,检查气密性;将20g粗产品放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液;
②打开弹簧夹C,在A处缓缓通入一段时间空气;
③称量 G的质量;
④关闭弹簧夹C,慢慢滴加浓盐酸直至D中无气泡冒出;
⑤打开弹簧夹C,再次缓缓通入一段时间空气;
⑥再次称量G的质量,得前后两次质量差为4.8g.
请回答下列问题
(2)
B装置的作用是,B装置中发生反应的化学方程式为.
(3)
在步骤②中,A处缓缓通入一段时间空气的目的是.
(4)
若没有H装置,测定的Na2CO3的质量分数会(填“偏大”、“偏小”、“不变”).
(5)
该兴趣小组指导老师认为该方案有些不合理,指导同学们更换了共中的一种试剂并去掉了一个装置后实验得到了改善,并测得20.0g粗产品只能产生4.4gCO2 . 你认为更换后的试剂是.原实验中实验值4.8g比正确值4.4g偏大的原因是(假设操作均正确).数据计算:根据正确值4.4g求得了样品中Na2CO3的质量分数.
2.
如图是实验室中常见的一些装置,请根据所学知识回答下列问题:
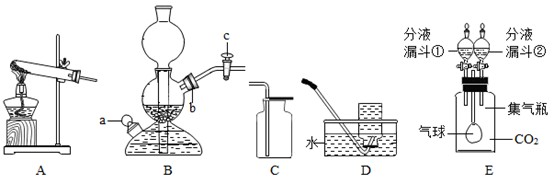
(1)
实验室用A装置制备氧气,反应的化学方程式是,若要收集较纯净的氧气,选择的收集装置是(填装置编号)。
(2)
实验室用B装置制备二氧化碳气体,实验开始前,应从(填“a”或“b”)处装入大理石,收集完气体后,(填操作),反应随后停止。
(3)
E装置的集气瓶中充满CO2 , 打开分液漏斗①,滴入少量NaOH浓溶液,气球明显胀大,写出反应的化学方程式;关闭分液漏斗①,打开分液漏斗②,气球恢复原状,则分液漏斗②中可能盛放的溶液是(填名称,忽略滴入液体体积)。
(4)
用盐酸和碳酸钙制备CO2产生了大量废液。通过以下探究制定废液处理方案。
I.探究废液成分。
推测废液所含溶质:推测一:CaCl2;推测二:CaCl2和HCl。
用一种药品验证哪种推测成立,可选择_____(填标号)
实验测得废液中的溶质是CaCl2和HCl。
A . NaOH溶液 B . AgNO3溶液 C . 锌粒 D . CuSO4溶液
(5)
Ⅱ.废液的处理:决定用Na2CO3除去它们。
【提出问题】如何估算Na2CO3固体的用量?
【进行实验】取100mL废液样品于烧杯中,逐滴滴加5.3%的Na2CO3溶液,用pH传感器测定滴加过程中溶液的pH。实验测得部分数据如图二所示。
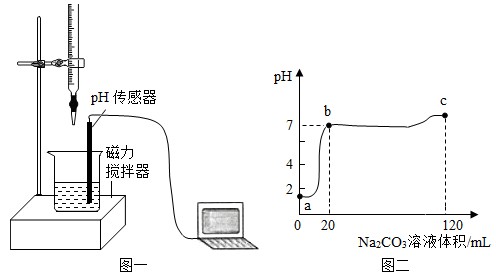
【结果讨论】
i.整个实验过程发生反应的化学方程式是、。
ii.c点时,将烧杯中的清液于试管中,滴加CaCl2溶液,有白色沉淀生成,说明处理100mL废液,所需5.3%的Na2CO3溶液的体积120mL。(填“大于”“等于”或“小于”)
iii.将烧杯中的沉淀过滤、洗涤、干燥、称重,质量为4g。若处理100mL该废液,理论上需要Na2CO3固体g。(实验所用Na2CO3溶液的密度近似看作1g/mL)
3.
实验室常用过氧化氢溶液和二氧化锰混合制取氧气。
(1)
计算用136g5%的过氧化氢溶液理论上可以制取氧气质量是多少?
(2)
用排水法收集的氧气质量一定小于理论值,原因可能是(写一条即可)。
1.
2022年北京冬奥会秉持绿色、共享、开放、廉洁理念,首次采用氢气作为火炬燃料。计算完全燃烧0.4kg氢气,理论上需要消耗氧气的质量是?
3.
某合金6g与足量的稀硫酸充分反应后,如果生成0.2g氢气,该合金中的元素可能是( )
A . Zn和Fe B . Cu和Au C . Zn和Cu D . Mg和Al
网址:某化工厂用3.7t的熟石灰处理溶质质量分数为2%的硫酸废液,待测得废液pH=7时再进行排放。理论上这些熟石灰可以处理硫酸废液质量是多少? https://www.yuejiaxmz.com/news/view/299888
相关内容
15.亚硫酸钠在空气中易被氧化生成硫酸钠.现有ag亚硫酸钠样品.溶解后加入足量氯化钡溶液.可得干燥沉淀bg. (1)若亚硫酸钠未被氧化.b= a. (2)若亚硫酸钠全被氧化.b= a.——青夏教育精英家教网——次氯酸钠在荧光液废水脱色处理中的应用
已知生活中厕所清洁剂的pH=1.厨房的清洁剂的pH=12.下列关于两者的说法不正确的是( )A. 厕所清洁剂加水稀释.溶液pH升高 B. 厨房清洁剂可能含有NaOHC. 混合使用能提高两者的清洁效果 D. 厕所清洁剂可能使铁制下水道腐蚀 C [解析]溶液的pH小于7.溶液呈酸性.pH越小.酸性越强,溶液的pH大于7.溶液呈碱性.pH越大碱性越强,pH等于7.溶液 题目和参考答案——青夏教育精英家教网——
回收利用是保护金属资源的一条有效途径.某工业废料含碱式碳酸铜[Cu2(OH)2CO3]和氧化铁.经过处理后可得到铜和硫酸亚铁溶液.主要流程如下.已知:Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑ Fe+Fe2(SO4)3=3FeSO4(1)过程Ⅰ中加入过量A的目的是使固体完全溶解.(2)过程Ⅱ中发生的置换反应是Fe+CuSO4 题目和参考答案——青夏教育精英家教网——
亚硝酸钠(NaNO2)是一种污染物.有毒.金属加工废切削液中常含此物质.人们常用以下方法来处理:第一步:NaNO2+NH4Cl=NH4NO2+NaCl 第二步:NH4NO2 △ . X↑+2H2O X的化学式为 . 题目和参考答案——青夏教育精英家教网——
工业上以黄铜矿(主要成分CuFeS2)为原料制备金属铜.有如下两种工艺.I.火法熔炼工艺.将处理过的黄铜矿加人石英.再通人空气进行焙烧.即可制得粗铜.(1)焙烧的总反应式可表示为2CuFeS2+ 2SiO2+5O2=2Cu+2FeSiO3+4SO2该反应的氧化剂是 .(2)下列处理SO2的方法.不合理的是 A高空排放 B用纯碱溶液吸收制备亚硫酸钠C用 题目和参考答案——青夏教育精英家教网——
硫代硫酸钠晶体(Na2S2O3·5H2O,M=248g·mol
人类的日常生活离不开酸.碱.盐三类物质.请回答下列问题:(1)山药中含有碱性皂角素.皮肤沾上会奇痒难忍.你认为可涂厨房中的 来止痒,(2)①酸奶,②肥皂水,③食盐水,是生活中常见的三种物质.酸奶能使紫色石蕊试液变红.肥皂水显碱性.食盐水的pH=7.它们的pH由小到大的顺序为 ,(3)在树木上涂刷含有硫磺粉的石灰浆.作用是 .(4)服用含有氢氧化铝的药物可以治疗胃酸 题目和参考答案——青夏教育精英家教网——
下列各组物质能在pH=1的无色溶液中大量共存的是( ) A.K2SO4
如图所示是生活中常见的金属物质.(1)如图所示生活用品中.主要是利用金属导热性的是C.(2)铝具有很好的抗腐蚀性.原因是4Al+3O2=2Al2O3.(3)某些化学兴趣小组用铁丝.铜丝.稀硫酸和硫酸铜溶液.验证铁.铜.银的金属活动性顺序.实验结束后同学们欲对该实验的废液进行探究.他们先看到废液呈蓝色的现象.认为废液中一定含有硫酸铜,还认为一定含有硫酸亚铁.依� 题目和参考答案——青夏教育精英家教网——

