氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。Ⅰ.制取氢气(1)甲醇和水蒸气制取氢气的过程中有下列反应:CH3OH(g)⇌CO(g)+2H2(
制作简易热气球:填充氦气或氢气,用绳子固定并点燃底部加热源。 #生活知识# #科技生活# #科学实验#
氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。
Ⅰ.制取氢气
(1)甲醇和水蒸气制取氢气的过程中有下列反应:
CH3OH(g)⇌CO(g)+2H2(g)ΔH=+9lkJ•mol-1
CO(g)+H2O(g)⇌CO2(g)+H2(g)ΔH=-41kJ•mol-1
写出以甲醇为原料制取氢气的热化学方程式
CH3OH(g)+H2O(g)⇌CO2(g)+3H2(g)ΔH=+50kJ•mol-1
CH3OH(g)+H2O(g)⇌CO2(g)+3H2(g)ΔH=+50kJ•mol-1
。(2)理论上,能提高H2平衡产率的措施有
升高温度(或降低压强)
升高温度(或降低压强)
(写出一条即可)。Ⅱ.储存氢气
硼氢化钠(NaBH4)是研究最广泛的储氢材料之一。
已知:i.B的电负性为2.0 H的电负性为2.1
ii.25℃下NaBH4在水中的溶解度为55g,NaBO2在水中的溶解度为0.28g
(3)向NaBH4水溶液中加入催化剂Ru/NGR后,能够迅速反应,生成偏硼酸钠(NaBO2)和氢气。写出该反应的化学方程式
NaBH4+2H2O
R
u
/
NGR
NaBO2+4H2↑
NaBH4+2H2O
R
u
/
NGR
NaBO2+4H2↑
。(4)在研究浓度对催化剂Ru/NGR活性的影响时,发现B点后(见图1)增加NaBH4的浓度,制氢速率反而不降,推断可能的原因是
NaBH4的浓度过高,导致催化剂活性降低
NaBH4的浓度过高,导致催化剂活性降低
。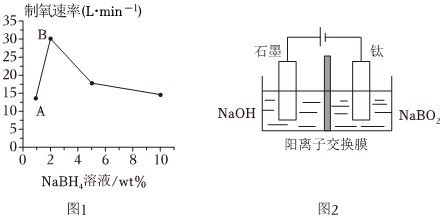
(5)用惰性电极电解NaBO2溶液可制得NaBH4,实现物质的循环使用,制备装置如图2所示。
①钛电极的电极反应式是
BO
-
2
+6H2O+8e-=
BH
-
4
+8OH-
BO
-
2
+6H2O+8e-=
BH
-
4
+8OH-
。②电解过程中,阴极区溶液pH
增大
增大
(填“增大”“减小”或“不变”)。【答案】CH3OH(g)+H2O(g)⇌CO2(g)+3H2(g)ΔH=+50kJ•mol-1;升高温度(或降低压强);NaBH4+2H2O
R
u
/
NGR
NaBO2+4H2↑;NaBH4的浓度过高,导致催化剂活性降低;
BO
-
2
+6H2O+8e-=
BH
-
4
+8OH-;增大
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/10/12 1:0:1组卷:14引用:1难度:0.6
相似题
1.肼(N2H4)可作为发射火箭的燃料。已知1g液态肼(N2H4)气体在空气中燃烧生成氮气和水蒸气,放出16.7kJ的热量,该反应的热化学方程式是( )
A.N2H4(l)+O2(g)═2H2O(g)+N2(g),△H=-16.7kJ•mol-1B.N2H4(l)+O2(g)═2H2O(l)+N2(g),△H=-534.4kJ•mol-1C.N2H4(l)+O2(g)═2H2O(g)+N2(g),△H=-534.4kJ•mol-1D.N2H4(l)+O2(g)═2H2O(g)+N2(g),△H=+534.4kJ•mol-1发布:2024/12/30 3:0:4组卷:126引用:9难度:0.6
2.氢在地球上主要以化合态的形式存在,是宇宙中分布最广泛的物质,它构成了宇宙质量的75%,属于二次能源.工业上生产氢的方式很多,常见的有水电解制氢,煤炭气化制氢,重油及天然气水蒸气催化制氢等.氢气是一种理想的绿色能源,如图1为氢能产生和利用的途径:
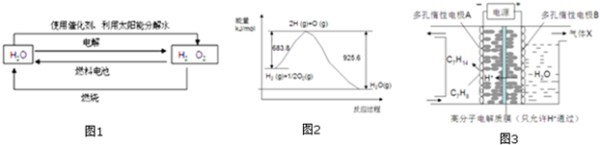
(1)图1的四个过程中能量转化形式有
A.2种 B.3种 C.4种 D.4种以上
(2)电解过程要消耗大量的电能,而使用微生物作催化剂在阳光下也能分解水.
2H2O(1)
通电
2H2(g)+O2(g)△H 1 2H2O(1)光照
催化剂
2H2(g)+O2(g)△H2以上反应的△H1△H2(选填“<”、“>”或“=”)
(3)已知H2O(l)→H2O(g)△H=+44kJ.mol-1,依据图2能量变化写出氢气燃烧生产液态水的热化学方程式
(4)氢能利用需要选择合适的储氢材料.
①NaBH4是一种重要的储氢载体,能与水反应生成NaBO2,且反应前后B的化合价不变,该反应的化学方程式为
②镧镍合金在一定条件下可吸收氢气生产氢化物:LaNi3(s)+3H2(g)═LaNi3H6(s)△H<0,欲使LaNi3H6(s)释放出气态氢,根据平衡移动的原理,可改变的条件之一是
③一定条件下,如图3所示装置可实现有机物的电化学储氢,使C7H8转化为C7H14,则电解过程中产生的气体X 为,电极A上发生的电极反应式为.
发布:2024/12/17 8:0:2组卷:38引用:1难度:0.5
3.在298K、1.01×105Pa下,将0.5mol CO2通入750mL 1mol•L-1NaOH溶液中充分反应,测得反应放出xkJ的热量。已知在该条件下,1mol CO2通入1L 2mol•L-1NaOH溶液中充分反应放出ykJ的热量,则CO2与NaOH溶液反应生成NaHCO3的热化学方程式正确的是( )
A.CO2(g)+NaOH(aq)═NaHCO3(aq)ΔH=-(2y-x)kJ•mol-1B.CO2(g)+NaOH(aq)═NaHCO3(aq)ΔH=-(2x-y)kJ•mol-1C.CO2(g)+NaOH(aq)═NaHCO3(aq)ΔH=-(4x-y)kJ•mol-1D.2CO2(g)+2NaOH(l)═2NaHCO3(l)ΔH=-(8x-2y)kJ•mol-1发布:2024/12/30 4:0:1组卷:147引用:5难度:0.7
相关试卷
网址:氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。Ⅰ.制取氢气(1)甲醇和水蒸气制取氢气的过程中有下列反应:CH3OH(g)⇌CO(g)+2H2( https://www.yuejiaxmz.com/news/view/1256282
相关内容
氢气是一种清洁高效能源,以甲醇为原料可以制取氢气。回答下列问题:(1)甲醇水蒸气重整制氢主反应:①CH3OH(g)CO(g)+2H2(g)ΔH=+90.7kJ/氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。已知:CH4(g)+H2O(g)=“===”CO(g)+3H2(g)H=“+206.2”kJ·mol
氢气是一种清洁能源.氢气的制取与储存是氢能源利用领域的研究热点.(1)以甲烷为原料制取氢气是工业上常用的制氢方法.已知:CH4(g)+H2O+3H2(g) ΔH=+206.2 kJ/molCH4——青夏教育精英家教网——
甲醇是人们开发和利用的一种新能源.已知:①2H2(g)+O2(g)═2H2O(l)△H1=
随着化石能源的减少.新能源的开发利用日益迫切.(1)Bunsen热化学循环制氢工艺由下列三个反应组成:SO2(g)+I2(g)+2H2O+H2SO4(l)△H=a kJ?mol
一氧化碳和氢气在443
开发使用清洁能源.发展“低碳经济 正成为科学家研究的主要课题.氢气.甲醇是优质的清洁燃料.可制作燃料电池.(1)甲烷水蒸气转化法制H2的主要转化反应如下:CH4(g) + H2O(g) CO(g) + 3H2(g)? △H=+206.2 kJ·mol
日常生活、生产中甲烷既是重要的清洁能源也是一种重要的化工原料。 (1)下图是CH4/H2O体系放氢焓变示意图: 则CH4(g)+CO2(g)=2CO(g)+2H2(g) △H= 。 (2)合成气(CO、H2)
日常生活、生产中甲烷既是重要的清洁能源也是一种重要的化工原料.(1)如图1是CH4/H2O体系放氢焓变示意图:则CH4(g)+CO2(g)=2CO(g)+2H2(g)△H=
科学家预测“氢能”将是未来最理想的新能源。请回答下列问题:(1)实验测得,1g氢气燃烧生成液态水放出142.9kJ热量,则表示氢气燃烧热的热化学方程式为

